Innehåll
Huvudskillnad
Atommassa och atomnummer är de två fraser som används i stor utsträckning i begreppen kemi och fysik. För att förstå vetenskapliga väsentliga faktorbegrepp bibehåller alla dessa fraser en hel betydelse. De flesta av de situationer som dessa två fraser är svåra för föräldrarna, de byter ut alla dessa fraser. Men de är just mycket ganska distinktiva från varandra, men alla dessa fraser bibehåller vissa likheter, men de är helt totalt annorlunda. Egenskaper och drag av olika tillhandahållande, ämnen och element kan inte förstås genom att förstå betydelsen av dessa fraser. Atommängd används som en metod för att tydligt definiera formen för ett material eller kanske substans är. Det redigeras och beskrivs som ett resultat av antalet protoner som finns i en kärnkälla medan alternativt atommassan faktiskt är den mängd som är associerad till alla protoner och dessutom neutroner som finns i hela den specifika kärnan associerad med. Elektroner väger verkligen inte väsentligt, därefter bestäms atommassan utan tvekan med tillsatsen av mängden associerad med protoner till neutroner. Dessutom kallas det atomvikten.
Vad är Atomic Mass?
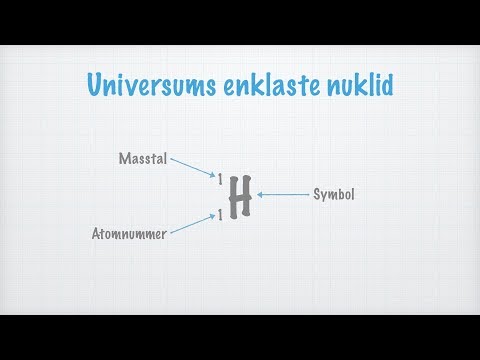
Massmängden eller vanligtvis kallad atommängd betecknas med (A) som vanligtvis är skriven på den övre sidan av den, det kallas dessutom atommängd eller kanske nukleonmängd, är faktiskt den slutliga ordmängden som involverar protoner och neutroner (som tillsammans kallas nukleoner) inuti en atomkärna. Den bestämmer den exakta atommassan hos atomer. På grund av de exakta verklighetsprotonerna och dessutom, neutroner var och en av dem är baryoner, den exakta massmängden A är jämförbar tillsammans med baryonmängden B eftersom den exakta kärnan i hela din atom och till och med jon. Massmängden är helt totalt annorlunda för varje distinkt isotop av den kemiska substansen. Detta är enbart inte motsvarande som ett resultat av atommängden (Z) Massmängden lanseras vanligtvis efter etablering eller kanske som ett superskript till vänster om din bild. För det mesta är den mest typiska isotopen som involverar kol faktiskt kol-12 eller 12C, som innehåller 6 protoner tillsammans med 6 neutroner. Det fullständiga isotopmärket kommer säkert också att ha den atomära mängden. Massmängden bör inte förväxlas med ett olika tillhörande tidsintervall vilken relativ atommassa av en.
Vad är atomnummer?
Atombeloppet betecknas med ”Z”. När det inkluderar kemi och dessutom fysik är normalt den atommängd som är förknippad med en kemikalie (dessutom kallad protonmängden) faktiskt antalet protoner som är helt placerade i hela kärnan associerad med en atom av det, och för det målet identiskt med tillhörande val av avgift av den specifika kärnan. Det är verkligen traditionellt symboliserat med bilden Z. Atommängden bestämmer fullständigt en kemikalie. Inom en oladdad atom kan den exakta atommängden motsvara antalet elektroner. Atommängden, Z, bör sluta felaktigt bekräftas som ett resultat av massmängden, A, som är antalet nukleoner, mängden neutroner, N, bekräftas som ett resultat av neutronmängden associerad med atomen; därefter A = Z + N (alla dessa delar kommer alltid att vara hela siffror). Eftersom protoner och dessutom neutroner har ungefär den ekvivalenta massan (tillsammans med massan av elektronerna är faktiskt försumbar för många kapaciteter), och dessutom är massan att dra tillbaka med nukleonbindning vanligtvis mindre jämfört med den exakta nukleonmassan, atomen, varje gång som indikeras inuti enstaka atommassamoder Atomer med exakt samma atommängd Z är ändå distinkta neutronnummer N, och därefter distinkta atomiska ton, märkta som isotoper.
Viktiga skillnader
- Atommängden representeras av "Z" medan atommassan representeras av "A".
- Atommassa definierar inte typen av medan Atommängd definierar typen av.
- Atommassa används för att peka helt olika isotoper av motsvarande medan det inte är fallet för atommängden.
- Atommassan mäts genom atommasseenheten (amu) medan atommängden helt enkelt är en mängd.
- Massor av elektroner är alltid lika med atommängden ändå inte lika med massmängden.
- Om atommängden är extrem betyder det att atommassan till och med är extrem.