Innehåll
- Huvudskillnad
- Jämförelsediagram
- Vad är joniska föreningar?
- Vad är molekylära föreningar?
- Joniska föreningar kontra molekylära föreningar
Huvudskillnad
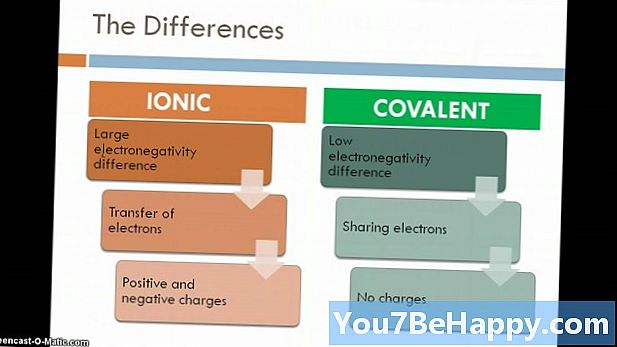
Förening känns igen som ett ämne som bildas när två eller flera element kombineras i bestämda proportioner genom en kemisk bindning. Jonisk förening är den förening som bildas på grund av elektrostatisk dragkraft mellan metaller och icke-metaller. Vanligtvis förekommer de joniska föreningarna i ett sålt kristallint tillstånd. Dessutom är joniska föreningar goda ledare för elektricitet och har höga smält- och kokpunkter. Å andra sidan bildas molekylära föreningar på grund av delning av elektroner mellan två icke-metaller. I förhållande till jonförening är de dålig elektrisk ledare och har låg smältpunkt och kokpunkt.
Jämförelsediagram
| Ioniska föreningar | Molekylära föreningar | |
| Bildning | Joniska föreningar bildas på grund av elektrostatisk attraktionskraft mellan metaller och icke-metaller. | Molekylära föreningar bildas på grund av delning av elektroner mellan två icke-metaller. |
| Grupp | Ioniska föreningar bildas mellan metall och icke-mental. | Molekylära föreningar bildas när två icke-metaller kemiskt kombineras |
| Obligation | Ionisk förening bildas på grund av elektrostatisk attraktionskraft som kallas jonisk bindning. | Molekylära föreningar bildas på grund av kovalent bindning mellan elementen. |
| Smältpunkt och kokpunkt | Hög | Låg |
| stat | Ioniska föreningar är alltid i fast tillstånd med bildande kristallint utseende. | Molekylära föreningar kan vara i vilket som helst tillstånd, fast, flytande eller gas vid rumstemperatur. |
| Ledare för elektricitet | Bra | Dålig |
Vad är joniska föreningar?
Dessa föreningar bildas på grund av elektrostatisk dragkraft mellan metaller och icke-metaller. I enklare ord får kraften (jonbindning) i detta positivt och negativt laddat reagera tillsammans för att skapa en förening. Vanligtvis förekommer de joniska föreningarna i ett sålt kristallint tillstånd och är goda elektriska ledare med höga smält- och kokpunkter. Joniska föreningar bildas mellan metaller och icke-metaller och har någon form av glänsande utseende.
Exempel: Bordsalt (NaCl) är det vanligaste exemplet på jonisk förening. I denna formation är natrium (NA) metall, medan klor (Cl) är icke-metall, båda hålls samman på grund av den elektrostatiska dragkraften mellan båda.
Vad är molekylära föreningar?
Föreningarna som bildas på grund av delning av elektroner mellan icke-metaller är kända som Molecular Compound. Elementen som reagerar här hålls samman på grund av den kovalenta bindningen, och det är därför dessa föreningar ofta kallas kovalenta föreningar.I förhållande till jonförening är de dålig elektrisk ledare och har låg smältpunkt och kokpunkt.
Exempel: I Ozone (O3) kombineras syre med delning av elektroner för att bilda Ozon.
Joniska föreningar kontra molekylära föreningar
- Joniska föreningar bildas på grund av elektrostatisk dragkraft mellan metaller och icke-metaller, medan molekylära föreningar bildas på grund av delning av elektroner mellan två icke-metaller.
- Molekylära föreningar bildas när två icke-metaller kemiskt kombinerar, å andra sidan bildas joniska föreningar mellan metall och icke-mental.
- Molekylära föreningar bildas på grund av kovalent bindning mellan element, medan jonisk förening bildas på grund av elektrostatisk attraktionskraft känd som jonisk bindning.
- Molekylära föreningar har låg smältpunkt och kokpunkt jämfört med joniska föreningar.
- Molekylära föreningar kan vara i vilket som helst tillstånd, fast, flytande eller gas vid rumstemperatur, medan joniska föreningar alltid är i fast tillstånd med bildande kristallint utseende.
- Molekylära föreningar är dålig elektrisk ledare, medan joniska föreningar är god elektrisk ledare.